2021年3月27日,“高博医学论坛——血液病及造血干细胞移植后肺部并发症的诊治进展研讨会”盛大召开,会议通过线上线下双通道,邀请到呼吸感染、检验、病原微生物、放射、血液肿瘤众多专家大咖共话血液病及造血干细胞移植后肺部并发症的诊治。会议上,北京大学人民医院呼吸与危重医学科卢冰冰教授就《造血干细胞移植患者合并闭塞性细支气管炎综合征(BOS)的诊治》进行了精彩分享。
一、认识BOS
造血干细胞移植(HSCT)术后慢性移植物抗宿主病(cGVHD)的发生,严重影响了患者的预后,如何预防和治疗cGVHD,一直是我们不断探索的方向。
cGVHD在肺部的表现包括两种形式,即累及小气道引起的阻塞性肺疾病(OLD)和累及肺间质引起限制性肺疾病(RLD),其组织病理学特征是小气道周围(OLD)或肺间质(RLD)的胶原沉积和进展性纤维化,并可导致患者的肺功能严重受损。目前,闭塞性细支气管炎(BO)是慢性GVHD在肺部的主要表现形式,这一观点已被学术界广泛接受。而另一方面,cGVHD相关的间质性肺疾病(ILD)的病理生理和临床特征目前尚缺乏充分的研究。这次卢教授带我们探讨的是cGVHD累及小气道并引起闭塞性细支气管炎综合征(BOS)的诊断和治疗。
淋巴细胞性细支气管炎(LB)和闭塞性细支气管炎(BO)均为组织病理学诊断。LB的组织学特点为供者来源的大量淋巴细胞浸润细支气管管壁,导致细支气管炎。LB患者的主要临床症状包括剧烈咳嗽、咳痰,可伴喘息或气道高反应,容易误诊为哮喘。这个阶段的细支气管炎对激素和免疫抑制剂治疗十分敏感,病程呈可逆性。闭塞性细支气管炎(BO)的组织学特点为细支气管粘膜下及细支气管旁纤维化,晚期细支气管管腔呈向心性狭窄或完全闭塞。BO患者的主要症状是进行性加重的活动性气短,起病隐匿,病程不可逆。其胸部HRCT表现为过度通气或“马赛克”征,晚期可见中央型支气管扩张。肺功能特点是呼气流速受限,阻塞性通气功能障碍。LB是BO历经发展的早期阶段,也是BO发生的高危因素。 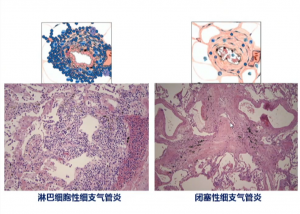
BO和BOS需要区分
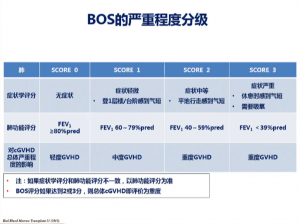
如前所述,确诊BO需要外科肺活检,这种侵入性检查对大多数HSCT患者不易实现,因此以临床以闭塞性细支气管炎综合征(BOS)来定义具有阻塞性气流受限特征的cGVHD-肺疾病。BOS的诊断标准:1)HSCT患者其他任一器官已确诊cGVHD;2)排除下呼吸道感染;3)肺功能:FEV1/FVC<70%、FEV1<75%pred且FEV1在2年内下降超过10% 。BOS的严重程度通过症状学评分及肺功能(FEV1%pred)评分共同判定,当症状学评分和肺功能评分不一致时,以肺功能评分(FEV1%pred)为准。只要肺功能评分达到2分或3分,则患者总体cGVHD即为重度。鉴于BO起病隐袭,患者就诊时往往肺功能严重受损,因此早期诊断尤为重要。建议对所有cGVHD患者的肺功能定期随访。
二、不同BOS患者治疗反应各有不同
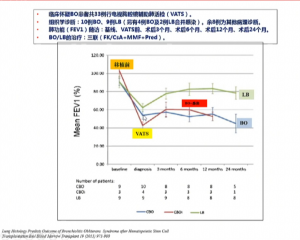
BOS是基于肺功能检查的临床诊断,不能等同于BO。BOS患者的小气道病理,既可能是供者淋巴细胞浸润(LB),也可能是气道壁纤维化(BO),或是二者不同程度的混合,只有经过治疗,才能明确转归。如前所述,LB患者对治疗比较敏感,而BO患者预后较差。2013年的一项临床研究证实了上述观点。该研究共纳入33例BOS患者,所有患者接受肺活检后结果显示:33例BOS患者中,包括10例BO、9例LB、 4例BO合并感染、2例LB合并感染、8例其他病理诊断。所有患者均接受包括他克莫司(FK)/环孢素(CsA)+霉酚酸酯(MMF)+激素的三联治疗,并定期随访肺功能。结果显示,BO患者肺功能逐渐趋于稳定,后期有小幅度下降;而LB患者肺功能得到明显改善,后期维持稳定。另外,随访期间,BO组患者死亡率50%(7/14),LB组患者死亡率9%(1/11)。综上所述, LB组患者预后显著优于BO。
三、BOS的主要治疗方案
卢教授结合自身的诊治经验,为大家详尽地介绍了BOS目前的治疗现状及注意事项。
一线治疗
二线治疗
钙调磷酸酶抑制剂——环孢素/他克莫司:二线治疗药物。如果患者在应用环孢素的情况下病情仍趋进展,建议转换为他克莫司。他克莫司药效显著强于环孢素,且患者耐受性较好。 硫唑嘌呤(AZA):二线治疗药物。卢教授认为此药临床疗效确切,但起效较慢,更适用于维持治疗,不宜用于快速进展的BOS。一部分患者因硫代嘌呤甲基转移酶(TPMT)的缺乏,导致AZA细胞毒作用增强,容易引起骨髓抑制。另外, AZA应避免与甲氨蝶呤(MTX)、MMF等联用,否则细胞毒作用将显著增强。 霉酚酸酯:二线治疗药物。单独应用疗效较弱,常与激素、环孢素/他克莫司联合应用。该药不宜与硫唑嘌呤联用,否则将过度抑制嘌呤的代谢。 阿奇霉素:小剂量阿奇霉素具有抗炎作用,建议BOS患者长期用药,疗程至少3月以上。
三线治疗
四、BOS的辅助支持治疗——吸入治疗
吸入治疗,包括吸入激素、吸入支气管扩张剂,均可以作为BOS的辅助治疗。由于研究证据质量不高,此类药物在cGVHD-BOS治疗中的推荐等级较弱。
五、总结
BOS是基于肺功能检查、以阻塞性气流受限为特征的cGVHD-肺疾病。患者的主要症状是进行性加重的活动后气短及活动耐力下降。BOS不等同于BO,因此存在治疗空间,主张积极治疗和随访。治疗采用以多种不同作用机制的药物联合治疗为主。治疗目标包括:
1)延缓肺功能下降; 2)维持肺功能稳定; 3)有限改善肺功能。
专家介绍

北京大学人民医院呼吸与危重医学科副主任医师 2012年曾在美国克利夫兰医学中心呼吸病研究所研修,主要研修方向包括呼吸危重症、肺间质疾病及肺移植。 多年来工作在临床一线,熟练掌握呼吸危重医学领域的基础理论及各种高级生命支持技术,擅长呼吸危重症救治。 专注于呼吸病学与其他医学专业之间交叉领域的研究进展,在弥漫性肺间质疾病、实体器官及造血干细胞移植相关肺部并发症、系统性疾病的肺部合并症、肺血管疾病等方面的规范化诊治方面具备扎实的理论基础和丰富的临床经验。
*内容来源:高博医学论坛——血液病及造血干细胞移植后肺部并发症的诊治进展大会 |